Việc thử tương đương sinh học của thuốc gồm những giai đoạn nào? Người tham gia thử tương đương sinh học của thuốc phải đáp ứng những yêu cầu gì?
Việc thử tương đương sinh học của thuốc gồm những giai đoạn nào?
Căn cứ Điều 96 Luật Dược 2016 quy định về các giai đoạn thử tương đương sinh học của thuốc và thuốc phải thử tương đương sinh học như sau:
Các giai đoạn thử tương đương sinh học của thuốc và thuốc phải thử tương đương sinh học
1. Thử tương đương sinh học của thuốc gồm các giai đoạn sau đây:
a) Giai đoạn nghiên cứu lâm sàng là giai đoạn thử nghiệm thuốc đối chứng và thuốc thử tương đương sinh học đã đạt yêu cầu về an toàn, hiệu quả để so sánh sinh khả dụng của 02 thuốc trên người tình nguyện;
b) Giai đoạn phân tích dịch sinh học của người là giai đoạn phân tích, xác định nồng độ thuốc đối chứng và thuốc thử tương đương sinh học trong mẫu sinh học của người tình nguyện sau khi được dùng ở giai đoạn nghiên cứu lâm sàng nhằm so sánh sinh khả dụng và chứng minh tính tương đương sinh học của 02 thuốc.
2. Thuốc generic phải thử tương đương sinh học khi có dược chất, dạng bào chế thuộc danh mục dược chất, dạng bào chế phải thử tương đương sinh học do Bộ trưởng Bộ Y tế ban hành.
Theo quy định trên, việc thử tương đương sinh học của thuốc gồm 02 giai đoạn sau:
+ Giai đoạn nghiên cứu lâm sàng: giai đoạn thử nghiệm thuốc đối chứng và thuốc thử tương đương sinh học đã đạt yêu cầu về an toàn, hiệu quả để so sánh sinh khả dụng của 02 thuốc trên người tình nguyện.
+ Giai đoạn phân tích dịch sinh học của người: giai đoạn phân tích, xác định nồng độ thuốc đối chứng và thuốc thử tương đương sinh học trong mẫu sinh học của người tình nguyện sau khi được dùng ở giai đoạn nghiên cứu lâm sàng nhằm so sánh sinh khả dụng và chứng minh tính tương đương sinh học của 02 thuốc.

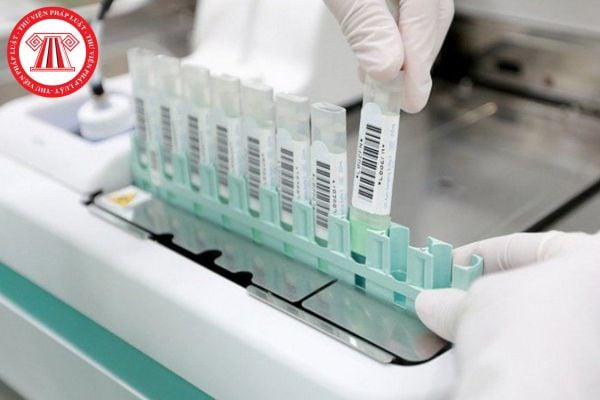
Thử tương đương sinh học của thuốc (Hình từ Internet)
Người tham gia thử tương đương sinh học của thuốc phải đáp ứng những yêu cầu gì?
Theo khoản 1 Điều 97 Luật Dược 2016 quy định về điều kiện của người tham gia thử tương đương sinh học của thuốc như sau:
Điều kiện, quyền và nghĩa vụ của người tham gia thử tương đương sinh học của thuốc
1. Người tham gia thử tương đương sinh học của thuốc phải đáp ứng điều kiện quy định tại Điều 90 của Luật này.
...
Cụ thể ở Điều 90 Luật Dược 2016 quy định về điều kiện của người tham gia thử thuốc trên lâm sàng như sau:
Điều kiện của người tham gia thử thuốc trên lâm sàng
1. Phải là người tình nguyện, đáp ứng yêu cầu chuyên môn của việc thử thuốc trên lâm sàng và phải ký thỏa thuận tình nguyện tham gia nghiên cứu với cơ sở kinh doanh dịch vụ thử thuốc trên lâm sàng, trừ người bị hạn chế năng lực hành vi dân sự, mất năng lực hành vi dân sự.
2. Trường hợp chưa đến tuổi thành niên, bị hạn chế năng lực hành vi dân sự, mất năng lực hành vi dân sự thì phải được sự đồng ý của người đại diện hoặc người giám hộ theo quy định của pháp luật.
3. Trường hợp là phụ nữ mang thai hoặc đang cho con bú, hồ sơ nghiên cứu phải ghi rõ lý do tuyển chọn và biện pháp phù hợp để bảo vệ người tham gia thử thuốc trên lâm sàng.
Theo đó, người tham gia thử tương đương sinh học của thuốc phải đáp ứng những yêu cầu được quy định tại Điều 90 nêu trên.
Quyền và nghĩa vụ của người tham gia thử tương đương sinh học của thuốc được quy định thế nào?
Theo khoản 2 Điều 97 Luật Dược 2016 quy định về quyền và nghĩa vụ của người tham gia thử tương đương sinh học của thuốc như sau:
Điều kiện, quyền và nghĩa vụ của người tham gia thử tương đương sinh học của thuốc
...
2. Quyền và nghĩa vụ của người tham gia thử tương đương sinh học của thuốc thực hiện theo quy định tại Điều 91 của Luật này.
Theo quy định tại Điều 91 Luật Dược 2016 về quyền và nghĩa vụ của người tham gia thử thuốc trên lâm sàng như sau:
Quyền và nghĩa vụ của người tham gia thử thuốc trên lâm sàng
1. Người tham gia thử thuốc trên lâm sàng có các quyền sau đây:
a) Trước khi thử thuốc, được cung cấp thông tin đầy đủ, trung thực và những rủi ro có thể xảy ra;
b) Được tổ chức, cá nhân có thuốc thử lâm sàng bồi thường thiệt hại nếu có thiệt hại do thử thuốc gây ra;
c) Được giữ bí mật về thông tin cá nhân có liên quan;
d) Không phải chịu trách nhiệm khi đơn phương chấm dứt việc tham gia thử thuốc trên lâm sàng;
đ) Khiếu nại, khởi kiện, tố cáo về hành vi vi phạm pháp luật của tổ chức, cá nhân có thuốc thử lâm sàng và nhận thử thuốc.
2. Người tham gia thử thuốc trên lâm sàng có nghĩa vụ tuân thủ hướng dẫn của nghiên cứu viên theo hồ sơ thử thuốc trên lâm sàng đã được phê duyệt.
Như vậy, người tham gia thử tương đương sinh học của thuốc có những quyền và nghĩa vụ được quy định tại Điều 91 nêu trên.
Trong đó có quyền được cung cấp thông tin đầy đủ, trung thực và những rủi ro có thể xảy ra trước khi thử thuốc.








Quý khách cần hỏi thêm thông tin về có thể đặt câu hỏi tại đây.
- Cơ sở lưu trú du lịch đáp ứng tối thiểu bao nhiêu lượt khách lưu trú thì được công nhận khu du lịch cấp tỉnh?
- Thông thầu bao gồm các hành vi nào? Người có hành vi thông thầu bị đi tù không? Mức phạt tù cao nhất đối với hành vi thông thầu?
- Thông quan là gì? Hàng hóa được thông quan khi nào? Cụ thể quyền, nghĩa vụ người khai hải quan?
- Tổ chức Đảng vi phạm về giải quyết khiếu nại, tố cáo gây hậu quả ít nghiêm trọng bị kỷ luật bằng hình thức khiển trách trong trường hợp nào?
- 7 hành vi bị nghiêm cấm đối với người khai hải quan là những hành vi nào theo pháp luật hải quan?









