Thực hành tốt thử thuốc trên lâm sàng là gì? Thực hành tốt thử thuốc trên lâm sàng phải đảm bảo các nguyên tắc nào?
Thực hành tốt thử thuốc trên lâm sàng là gì?
Theo khoản 2 Điều 3 Thông tư 29/2018/TT-BYT quy định như sau:
Thực hành tốt thử thuốc trên lâm sàng (Good Clinical Practice - GCP) là bộ nguyên tắc, tiêu chuẩn cho việc thiết kế, tổ chức triển khai, thực hiện, giám sát, kiểm tra, ghi chép, phân tích và báo cáo về thử thuốc trên lâm sàng nhằm bảo đảm tính tin cậy, chính xác của dữ liệu và báo cáo kết quả nghiên cứu, bảo vệ quyền, sự an toàn và bảo mật thông tin của đối tượng nghiên cứu.
Theo đó, Thực hành tốt thử thuốc trên lâm sàng là bộ nguyên tắc, tiêu chuẩn cho việc thiết kế, tổ chức triển khai, thực hiện, giám sát, kiểm tra, ghi chép, phân tích và báo cáo về thử thuốc trên lâm sàng nhằm bảo đảm tính tin cậy, chính xác của dữ liệu và báo cáo kết quả nghiên cứu, bảo vệ quyền, sự an toàn và bảo mật thông tin của đối tượng nghiên cứu.
Lưu ý: Thực hành tốt thử thuốc trên lâm sàng được viết tắt từ Good Clinical Practice - GCP.

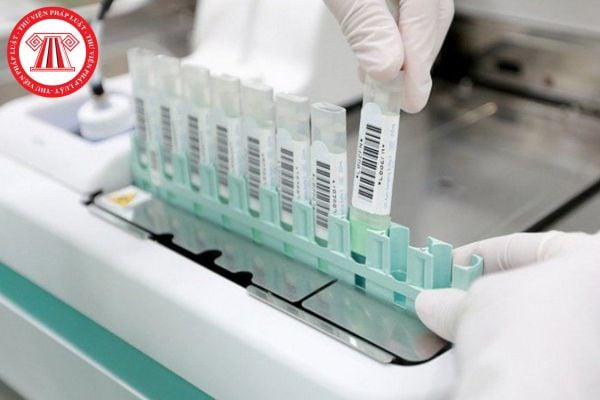
Thực hành tốt thử thuốc trên lâm sàng (Hình từ Internet)
Thực hành tốt thử thuốc trên lâm sàng phải đảm bảo các nguyên tắc nào?
Căn cứ theo Điều 4 Thông tư 29/2018/TT-BYT quy định như sau:
Nguyên tắc, tiêu chuẩn Thực hành tốt thử thuốc trên lâm sàng
1. Ban hành nguyên tắc, tiêu chuẩn Thực hành tốt thử thuốc trên lâm sàng tại Phụ lục I kèm theo Thông tư này và tài liệu cập nhật quy định tại khoản 2 Điều này trên cơ sở tham khảo hướng dẫn của ICH, WHO và các cơ quan quản lý tham chiếu quy định tại khoản 5 Điều 3 Thông tư này.
2. Trường hợp ICH và WHO sửa đổi, bổ sung nguyên tắc, tiêu chuẩn GCP (tài liệu cập nhật), Cục Khoa học công nghệ và Đào tạo cập nhật và công bố tài liệu cập nhật trên Cổng thông tin điện tử của Bộ Y tế và Trang thông tin điện tử của Cục Khoa học công nghệ và Đào tạo để các đối tượng có liên quan tra cứu, cập nhật và áp dụng.
Theo đó, Thực hành tốt thử thuốc trên lâm sàng phải đảm bảo các nguyên tắc sau:
- Ban hành nguyên tắc Thực hành tốt thử thuốc trên lâm sàng tại Phụ lục I kèm theo Thông tư này và tài liệu cập nhật quy định tại khoản 2 Điều này trên cơ sở tham khảo hướng dẫn của ICH, WHO và các cơ quan quản lý tham chiếu quy định tại khoản 5 Điều 3 Thông tư này.
- Trường hợp ICH và WHO sửa đổi, bổ sung nguyên tắc GCP (tài liệu cập nhật), Cục Khoa học công nghệ và Đào tạo cập nhật và công bố tài liệu cập nhật trên Cổng thông tin điện tử của Bộ Y tế và Trang thông tin điện tử của Cục Khoa học công nghệ và Đào tạo để các đối tượng có liên quan tra cứu, cập nhật và áp dụng.
Những đối tượng nào phải áp dụng nguyên tắc Thực hành tốt thử thuốc trên lâm sàng?
Tại Điều 5 Thông tư 29/2018/TT-BYT quy định cụ thể:
Đối tượng áp dụng nguyên tắc, tiêu chuẩn Thực hành tốt thử thuốc trên lâm sàng
1. Cơ sở thử thuốc trên lâm sàng triển khai áp dụng và đáp ứng GCP quy định tại Phụ lục I ban hành kèm theo Thông tư này và tài liệu cập nhật.
2. Trường hợp cơ sở kinh doanh dịch vụ thử tương đương sinh học của thuốc và các cơ sở có hoạt động nhận thử tương đương sinh học của thuốc không vì mục đích thương mại không đáp ứng GCP đối với giai đoạn nghiên cứu trên lâm sàng thì phải ký hợp đồng hoặc văn bản liên kết với cơ sở thử thuốc trên lâm sàng đáp ứng GCP quy định tại Phụ lục I ban hành kèm theo Thông tư này và tài liệu cập nhật để thực hiện giai đoạn nghiên cứu trên lâm sàng.
3. Cơ sở thử thuốc trên lâm sàng áp dụng tài liệu GCP cập nhật theo quy định tại khoản 2 Điều 4 Thông tư này trong thời hạn 12 tháng đối với trường hợp có yêu cầu thay đổi về cơ sở vật chất phục vụ việc thử thuốc hoặc 06 tháng đối với cập nhật khác, tính từ thời điểm tài liệu cập nhật được Cục Khoa học công nghệ và Đào tạo công bố trên Cổng thông tin điện tử của Bộ Y tế và Trang thông tin điện tử của Cục Khoa học công nghệ và Đào tạo.
Theo đó, những đối tượng phải áp dụng nguyên tắc Thực hành tốt thử thuốc trên lâm sàng gồm:
Thứ 1: Cơ sở thử thuốc trên lâm sàng triển khai áp dụng và đáp ứng GCP quy định tại Phụ lục I ban hành kèm theo Thông tư này và tài liệu cập nhật.
Thứ 2: Trường hợp cơ sở kinh doanh dịch vụ thử tương đương sinh học của thuốc và các cơ sở có hoạt động nhận thử tương đương sinh học của thuốc không vì mục đích thương mại không đáp ứng GCP đối với giai đoạn nghiên cứu trên lâm sàng thì phải ký hợp đồng hoặc văn bản liên kết với cơ sở thử thuốc trên lâm sàng đáp ứng GCP quy định tại Phụ lục I ban hành kèm theo Thông tư này và tài liệu cập nhật để thực hiện giai đoạn nghiên cứu trên lâm sàng.
Thứ 3: Cơ sở thử thuốc trên lâm sàng áp dụng tài liệu GCP cập nhật theo quy định tại khoản 2 Điều 4 Thông tư này trong thời hạn 12 tháng đối với trường hợp có yêu cầu thay đổi về cơ sở vật chất phục vụ việc thử thuốc hoặc 06 tháng đối với cập nhật khác, tính từ thời điểm tài liệu cập nhật được Cục Khoa học công nghệ và Đào tạo công bố trên Cổng thông tin điện tử của Bộ Y tế và Trang thông tin điện tử của Cục Khoa học công nghệ và Đào tạo.








Quý khách cần hỏi thêm thông tin về có thể đặt câu hỏi tại đây.
- Thanh tra thuế là gì? Được gia hạn thời hạn thanh tra thuế trong các trường hợp nào theo quy định?
- Khai thuế, tính thuế là gì? Địa điểm khai thuế, tính thuế của người nộp thuế là ở đâu theo quy định?
- Quyết định kết nạp đảng viên của cấp ủy có thẩm quyền Mẫu 9-KNĐ? Xây dựng, thực hiện kế hoạch kết nạp đảng viên ở chi bộ thế nào?
- Thông tin người nộp thuế là thông tin do người nộp thuế cung cấp hay do cơ quan thuế thu thập được?
- Giáo viên chủ nhiệm có được tham dự các cuộc họp của Hội đồng kỷ luật học sinh? Giáo viên có được làm chủ tịch Hội đồng kỷ luật học sinh?









