Điều kiện kinh doanh Dịch vụ gia công trang thiết bị y tế là gì? Hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế bao gồm những gì?
Abutment có phải là trang thiết bị y tế không?
Căn cứ tại khoản 1 Điều 2 Nghị định 98/2021/NĐ-CP quy định như sau:
1. Trang thiết bị y tế là các loại thiết bị, vật tư cấy ghép, dụng cụ, vật liệu, thuốc thử và chất hiệu chuẩn in vitro, phần mềm (software) đáp ứng đồng thời các yêu cầu sau đây:
a) Được sử dụng riêng lẻ hay phối hợp với nhau theo chỉ định của chủ sở hữu trang thiết bị y tế để phục vụ cho con người nhằm một hoặc nhiều mục đích sau đây:
- Chẩn đoán, ngăn ngừa, theo dõi, điều trị và làm giảm nhẹ bệnh tật hoặc bù đắp tổn thương, chấn thương;
- Kiểm tra, thay thế, điều chỉnh hoặc hỗ trợ giải phẫu và quá trình sinh lý;
- Hỗ trợ hoặc duy trì sự sống;
- Kiểm soát sự thụ thai;
- Khử khuẩn trang thiết bị y tế;
- Cung cấp thông tin cho việc chẩn đoán, theo dõi, điều trị thông qua biện pháp kiểm tra các mẫu vật có nguồn gốc từ cơ thể con người.
b) Không sử dụng cơ chế dược lý, miễn dịch hoặc chuyển hóa trong hoặc trên cơ thể người hoặc nếu có sử dụng các cơ chế này thì chỉ mang tính chất hỗ trợ để đạt mục đích quy định tại điểm a khoản này.
Theo đó, Abutment là viết tắt của Abutment Implant (hay còn gọi là vít hoặc khớp nối) là một trong ba bộ phận quan trọng trong cấu tạo của một chiếc răng implant.
Abutment đóng vai trò như một vật kết nối bắt buộc giữa trụ chân răng Implant và mão răng giả ở trên. Vì vậy, Abutment được xem là trang thiết bị y tế.
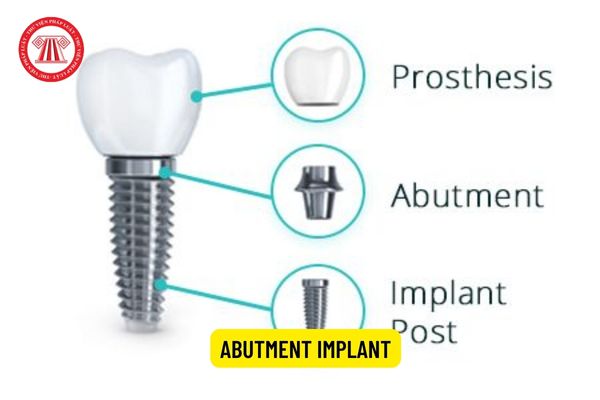
Abutment Implant (Hình từ Internet)
Điều kiện kinh doanh Dịch vụ gia công trang thiết bị y tế là gì?
Khi kinh doanh dịch vụ gia công sản xuất thiết bị y tế, ngoài việc đăng ký thành lập doanh nghiệp, Doanh nghiệp còn phải đáp ứng đủ điều kiện sau:
Căn cứ tại Điều 8 Nghị định 98/2021/NĐ-CP quy định:
Điều kiện về quản lý chất lượng của cơ sở sản xuất trang thiết bị y tế
1. Đạt tiêu chuẩn hệ thống quản lý chất lượng ISO 13485.
2. Đối với cơ sở sản xuất trang thiết bị y tế có chứa chất ma túy và tiền chất, ngoài việc đáp ứng các điều kiện quy định tại khoản 1 Điều này, phải đáp ứng thêm các yêu cầu sau đây:
a) Có hệ thống theo dõi quản lý quá trình xuất, nhập, tồn kho, sử dụng nguyên liệu là chất ma túy và tiền chất, quá trình xuất, nhập, tồn kho trang thiết bị y tế, nguyên liệu có chứa chất ma túy và tiền chất;
b) Trang thiết bị y tế, nguyên liệu có chứa chất ma túy và tiền chất được bảo quản ở một khu vực riêng trong kho hoặc kho riêng, phải bảo đảm an toàn.”
Theo đó, cơ sở sản xuất phải đáp ứng điều kiện nêu trên. Đồng thời phải làm thủ tục công bố đủ điều kiện sản xuất trang thiết bị y tế theo Điều 11 Nghị định 98/2021/NĐ-CP, cụ thể:
Thủ tục công bố đủ điều kiện sản xuất trang thiết bị y tế
1. Trước khi thực hiện sản xuất trang thiết bị y tế, cơ sở sản xuất trang thiết bị y tế có trách nhiệm nộp hồ sơ công bố về Sở Y tế nơi đặt địa điểm sản xuất (việc xác định địa điểm sản xuất được dựa vào địa điểm ghi trong giấy chứng nhận hệ thống quản lý chất lượng). Trường hợp có nhiều địa điểm sản xuất tại nhiều tỉnh khác nhau thì phải thực hiện việc công bố theo từng tỉnh.
2. Khi nhận hồ sơ (bao gồm cả giấy tờ xác nhận đã nộp phí theo quy định của Bộ Tài chính), Sở Y tế trên địa bàn nơi đặt cơ sở sản xuất trang thiết bị y tế đăng tải công khai trên Cổng thông tin điện tử về quản lý trang thiết bị y tế các thông tin và hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế.
3. Trong quá trình hoạt động cơ sở sản xuất có trách nhiệm lập văn bản thông báo sự thay đổi kèm theo các tài liệu liên quan đến thay đổi và cập nhật các tài liệu đó vào hồ sơ công bố đã công khai trên Cổng thông tin điện tử về quản lý trang thiết bị y tế trong thời hạn 03 ngày làm việc, kể từ ngày có sự thay đổi các thông tin trong hồ sơ công bố.
Theo đó, trước khi hoạt động, doanh nghiệp sản xuất phải nộp hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế về Sở Y tế nơi đặt địa điểm sản xuất (việc xác định địa điểm sản xuất được dựa vào địa điểm ghi trong giấy chứng nhận hệ thống quản lý chất lượng). Trường hợp có nhiều địa điểm sản xuất tại nhiều tỉnh khác nhau thì phải thực hiện việc công bố theo từng tỉnh.
Hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế bao gồm những gì?
Căn cứ tại Điều 9 Nghị định 98/2021/NĐ-CP quy định về hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế như sau:
- Hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế gồm:
+ Văn bản công bố đủ điều kiện sản xuất.
+ Giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng ISO 13485 được cấp bởi tổ chức đánh giá sự phù hợp theo quy định của pháp luật.
+ Các giấy tờ chứng minh đáp ứng điều kiện quy định tại khoản 2 Điều 8 Nghị định này.
Bên cạnh đó, Điều 10 Nghị định 98/2021/NĐ-CP cũng quy định về yêu cầu đối với hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế như sau:
- Hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế làm thành 01 bộ, trong đó:
+ Các tài liệu trong hồ sơ được in rõ ràng, sắp xếp theo trình tự theo quy định tại Điều 9 Nghị định này; giữa các phần có phân cách, có trang bìa và danh mục tài liệu.
+ Trường hợp tài liệu không bằng tiếng Anh hoặc không bằng tiếng Việt thì phải dịch ra tiếng Việt. Bản dịch phải được chứng thực theo quy định của pháp luật.
- Yêu cầu đối với một số giấy tờ trong bộ hồ sơ công bố đủ điều kiện sản xuất:
+ Bản gốc hoặc bản sao có chứng thực hoặc bản sao có xác nhận của cơ sở đề nghị công bố đủ điều kiện sản xuất đối với Giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng.
+ Bản gốc có xác nhận của cơ sở đề nghị công bố đủ điều kiện sản xuất đối với tài liệu chứng minh đáp ứng điều kiện quy định tại khoản 2 Điều 8 Nghị định 98/2021/NĐ-CP.









Quý khách cần hỏi thêm thông tin về có thể đặt câu hỏi tại đây.
- Mẫu Báo cáo số hóa hồ sơ thủ tục hành chính theo cơ chế một cửa, một cửa liên thông tại cơ quan thuế?
- Mức tiền hỗ trợ đối với diện tích đất nông nghiệp bị Nhà nước thu hồi là bao nhiêu? Có được hỗ trợ vay vốn tín dụng khi bị thu hồi không?
- Khi nào phải khai báo Mẫu số 05 - Tờ khai sử dụng máy photocopy màu, máy in có chức năng photocopy màu?
- Doanh nghiệp mua xe cũ của khách hàng để bán lại có cần sang tên xe từ khách hàng qua công ty không?
- Sửa đổi Nghị định 24/2024/NĐ-CP về lựa chọn nhà thầu hướng dẫn Luật Đấu thầu 2023 theo dự thảo thế nào?









